高校化学で頻出の「燃料電池」を、化学反応式や電子の流れを図解付きでわかりやすく解説します。負極・正極の反応式、リン酸形とアルカリ形の違い、テスト対策のポイントまで基礎から丁寧に学べます。
燃料電池とは?水素と酸素から電気を作る仕組みをわかりやすく解説
燃料電池(Fuel Cell)とは、水素と酸素を化学反応させて、直接「電気」を取り出す装置のことです。
燃料電池とは、水素と酸素を化学反応させることで電気を取り出す発電装置です。火を使って燃やす「燃焼」とは異なり、化学エネルギーを直接電気エネルギーへ変換するため、高い発電効率を持っています。
基本的な仕組みでは、負極側に水素、正極側に酸素を供給します。すると負極では水素が電子を放出して水素イオンになり、放出された電子が外部回路を流れることで電流が発生します。電子は正極へ移動し、酸素と水素イオンと結びついて水が生成されます。
燃料電池の大きな特徴は、発電時に二酸化炭素をほとんど排出しない点です。そのため、環境に優しい次世代エネルギーとして注目されています。
【高校化学】燃料電池の化学反応式(負極・正極)の作り方と酸化還元
仕組みの根本にあるのは、中学校の理科で習った「水の電気分解」の逆の反応です。
水の電気分解:水に電気を流すと、水素と酸素に分かれる。
燃料電池:水素と酸素を反応させると、水と電気が生まれる。
高校化学のテストで最もよく出題されるのが、各電極(負極・正極)で起きている「酸化還元反応」の式です。ここでは、代表的なリン酸形燃料電池(酸性の電解質を用いたもの)を例に、イオンと電子の動きを見てみましょう。
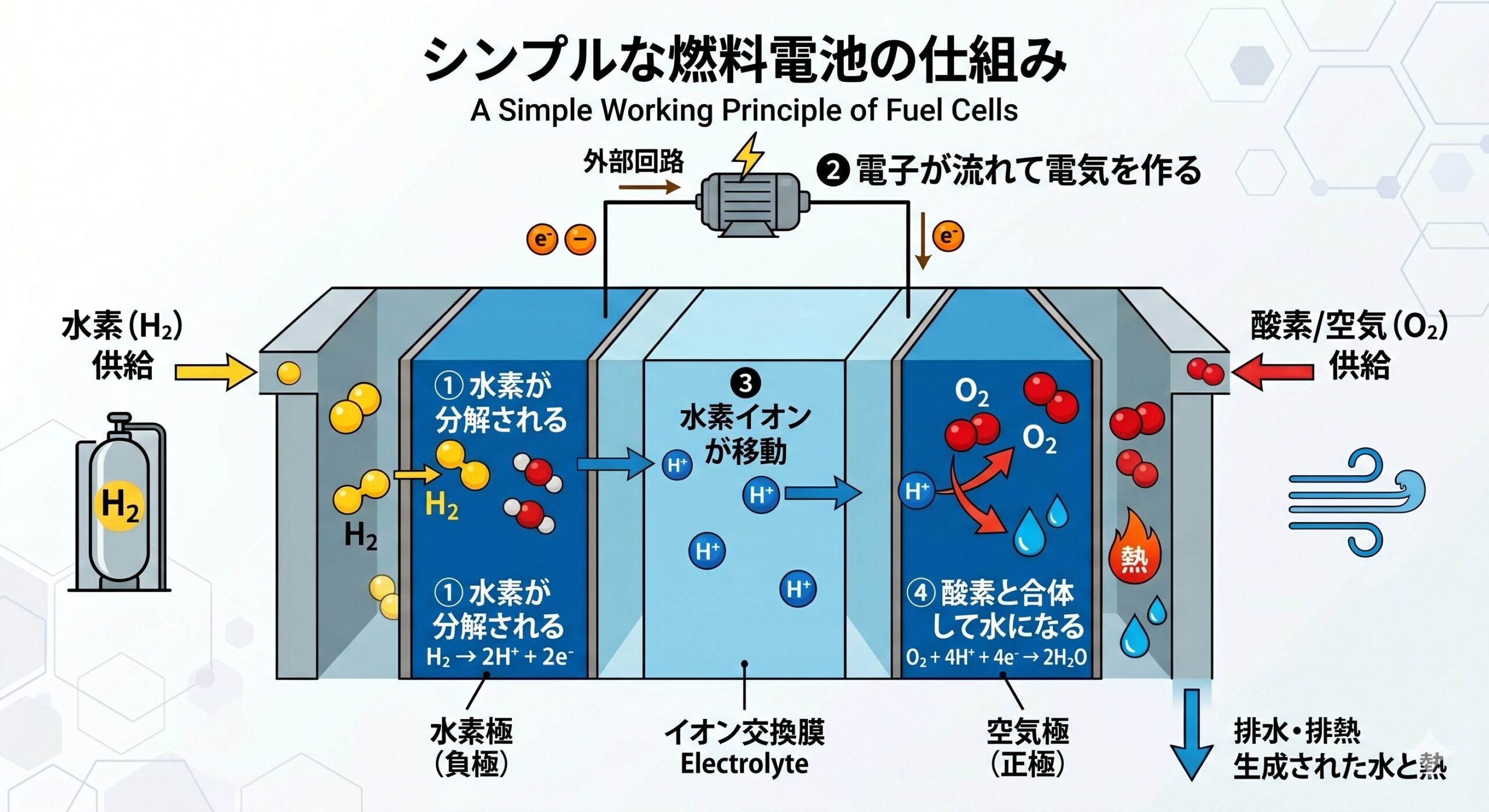
1. 負極(水素極)で起きる反応:酸化
負極には燃料である水素(H2)が供給されます。水素分子は触媒の働きによって電子(e–)を手放し、水素イオン(H+)に変化します。
負極の反応式:
H2→2H++2e–
2. 電子の移動(これが電気になる!)
負極で手放された電子(e–)は、導線(外部回路)を通って正極へと移動します。この「電子の流れ」こそが「電流(電気)」として、モーターを回したりライトを点灯させたりするエネルギーになります。
3. 正極(空気極)で起きる反応:還元
正極には空気中の酸素(O2)が供給されています。導線を通ってきた電子(e–)と、電解質の中を移動してきた水素イオン(H+)、そして酸素が結合して、水(H2O)が作られます。
正極の反応式:
O2+4H++4e–→2H2O
4. 全体の化学反応式
負極と正極の反応式を足し合わせて電子(e–)を消去すると、燃料電池全体の反応式になります。(負極の式を2倍して足し合わせます)
全体の反応式:
2H2+O2→2H2O
テストに出る!リン酸形とアルカリ形燃料電池の違いと反応式
燃料電池にはさまざまな種類がありますが、高校化学では「リン酸形燃料電池」と「アルカリ形燃料電池」がよく登場します。
リン酸形燃料電池
リン酸水溶液を電解質として利用する燃料電池です。
負極:
H2→2H++2e–
正極:
O2+4H++4e–→2H2O
酸性条件で反応が進行するのが特徴です。
アルカリ形燃料電池
水酸化カリウム水溶液などを電解質として使用します。
負極:
H2+2OH–→2H2O+2e–
正極:
O2+2H2O+4e–→4OH–
アルカリ性条件で反応が進む点がリン酸形との大きな違いです。
テストでは、「酸性かアルカリ性か」「生成するイオンは何か」を整理して覚えることが重要です。
燃料電池のメリット・デメリットは?環境問題と発電効率の課題
メリット
- 発電効率が高い
- 発電時に二酸化炭素の排出が少ない
- 騒音や振動が小さい
- 水素を利用するため次世代エネルギーとして期待されている
デメリット
- 水素の製造や輸送にコストがかかる
- 水素の貯蔵が難しい
- 装置価格が高い
- 水素製造時に化石燃料を使用するとCO₂が発生する場合がある
そのため、再生可能エネルギーを利用した「グリーン水素」の開発が進められています。
燃料電池の身近な実用例!自動車(FCV)や家庭用エネファーム
燃料電池自動車(FCV)
燃料電池を利用してモーターを動かす自動車です。代表例としては、
- トヨタ「ミライ」
- ホンダ「CR-V e:FCEV」
などがあります。
走行時に排出されるのは主に水だけであり、環境負荷が小さい点が特徴です。
家庭用燃料電池「エネファーム」
家庭で都市ガスから水素を取り出し、発電と給湯を同時に行うシステムです。
発電時に発生した熱をお湯として利用できるため、エネルギーを効率よく活用できます。
燃料電池が注目される理由とは?カーボンニュートラルとの関係
近年、燃料電池が世界中で注目されている理由の一つが、「カーボンニュートラル」の実現に役立つと考えられているためです。カーボンニュートラルとは、二酸化炭素(CO₂)の排出量と吸収量を実質的にゼロにする考え方を指します。
現在の火力発電では、石炭や石油、天然ガスなどの化石燃料を燃焼させるため、多くのCO₂が排出されます。一方、燃料電池は水素と酸素の化学反応によって発電するため、発電時に排出されるのは主に水だけです。そのため、地球温暖化対策として期待されています。
また、太陽光発電や風力発電と組み合わせる研究も進められています。再生可能エネルギーで作った電気を利用して水素を製造し、その水素を燃料電池に利用できれば、より環境負荷の少ないエネルギー循環が可能になります。
さらに、燃料電池は発電効率が高く、災害時の非常用電源としても活用できる点が注目されています。実際に、病院や避難施設、家庭用設備などで導入が進められており、今後のエネルギー社会を支える重要な技術の一つとして期待されています。
【まとめ】燃料電池の仕組みを反応式からしっかりと理解しよう
燃料電池は、水素と酸素の化学反応を利用して電気を取り出す発電装置です。
高校化学では、負極・正極での酸化還元反応式や電子の流れを理解することが重要になります。
特にリン酸形とアルカリ形では、反応に関わるイオンが異なる点が頻出ポイントです。
反応式を整理しながら、燃料電池の仕組みをしっかり身につけておきましょう。



コメント